|
|

|
|
ASÍ FUNCIONA LA LUZ
Texto e ilustraciones José Antonio E. García Álvarez
|
|
|
|
Como ya conocemos, las ondas de luz visible constituyen en sí una forma de energía. En realidad la luz se compone de infinidad de partículas muy pequeñas, carentes de masa, denominada “fotones”.
Los átomos son los encargados de liberar fotones de luz, pero para que eso suceda alguno de sus electrones tienen que ser primeramente excitado.
|
|
|
|
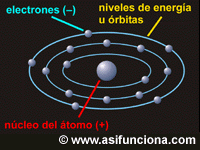
En cualquier átomo los electrones giran siempre dentro de uno o más niveles de energía denominados órbitas, de forma similar a como giran los planetas alrededor del
Sol. Para que los electrones (con carga negativa) se mantengan girando en sus
propias órbitas sin abandonarlas cambiando de un nivel de energía a otro, el núcleo del átomo (con carga positiva) ejerce una fuerte influencia para retenerlos.
|
|
Electrones girando alrededor del núcleo de un. átomo de fósforo (P). |
|
|
Por tanto, resulta prácticamente imposible que un electrón por sí
solo abandone la órbita en la que se mantiene girando para desplazarse a otro nivel de energía u órbita más externa.
|
Los electrones que giran en las órbitas más externas o alejadas del núcleo del átomo poseen mayor cantidad de energía que los que giran más
cercanos a éste. Como la influencia que
en ese caso ejerce la atracción del núcleo sobre ellos es más débil, son estos los más propensos a abandonar su órbita.
No obstante, cuando un átomo pierde un electrón por influencia de cualquier factor externo, ya sea físico o químico, su tendencia natural es recuperarlo de inmediato para poder continuar manteniendo un equilibrio eléctrico neutro, es decir, con la misma cantidad de electrones
(negativos), que de protones (positivos).
Para que se produzca un fotón de luz, es necesario que alguna partícula
ajena al átomo choque con uno de sus electrones en movimiento. Ese choque provocará
que éste se excite, haciendo que abandone su correspondiente
órbita y pase a ocupar, por breves instantes, otra órbita de un nivel superior
de energía y más alejada del núcleo del átomo al
cual pertenece. |
|
La reacción inmediata del núcleo del átomo será atraer el electrón para incorporarlo de nuevo a su órbita original. En el preciso instante que el
electrón regresa a su órbita, la energía extra que adquirió al pasar de un
nivel inferior a otro nivel superior de energía u órbita más externa, la
libera en forma de fotón de luz.
|
Ya conocemos que la luz blanca se compone de rayos de diferentes colores, cada uno con su propia longitud
de onda, frecuencia y cantidad de energía. Por tanto, el color de la luz
del fotón que emite el electrón cuando se reincorpora a su órbita original después de haber sido excitado, dependerá de la cantidad de energía que libere en ese momento, del elemento químico que le corresponde al átomo
a que pertenece y el nivel de energía u órbita donde se encontraba
éste girando en el momento que fue excitado (recordemos que los electrones que giran en las órbitas más cercanas al núcleo del átomo poseen menos energía que los que giran en las órbitas más
alejadas).
El color de la luz que emita un fotón se corresponderá siempre con la
frecuencia y longitud de onda propia de ese color y será perceptible para
nuestra vista siempre y cuando se encuentre dentro del rango fijado para
los rayos que cubren el espectro electromagnético de luz visible.
No obstante, existen también otros fotones que
emiten rayos de luz invisibles para nuestro sentido de la vista y que son de uso muy común.
Entre estos se encuentran los rayos infrarrojos (IR) utilizado en comunicaciones
inalámbricas, alarmas, mandos a distancia, etc. y los rayos
ultravioletas, comúnmente conocidos como rayos UVA, muy empleados como
bronceador de la piel. Dentro del espectro de ondas electromagnéticas los
rayos infrarrojos están situados antes del color de luz roja visible y
los ultravioletas a continuación del color violeta de luz visible .
Este es, a grandes rasgos, el principio en el cual se basa la emisión de fotones
de luz por los átomos.
En la práctica se utilizan diferentes técnicas para excitar los electrones,
de forma que produzcan luz artificial.
|
Favor de evaluar este tema
|
|

